보내는 기사
美 FDA 자문기구, 존슨앤드존슨 긴급사용 승인 권고
이미 가입된 회원입니다.
만 14세 이상만 회원으로 가입하실 수 있습니다.
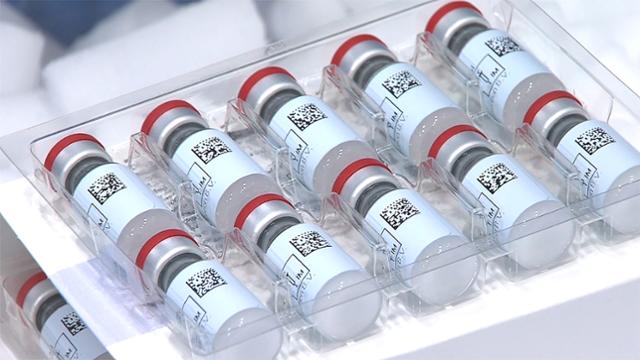
미국 제약사 존슨앤드존슨의 코로나19 백신. 로이터 연합뉴스
미국 식품의약국(FDA)의 자문기구가 26일(현지시간) 자국 제약사 존슨앤드존슨(J&J)의 신종 코로나바이러스 감염증(코로나19) 백신에 대해 긴급사용 승인(EUA)을 권고했다. 이변이 없는 한 FDA는 자문기구 권고에 따라 승인 결정을 내릴 것으로 미 언론들은 내다봤다. J&J 백신이 미국 내 세 번째 코로나19 백신이 되면 접종 속도도 한층 빨라질 전망이다.
미 CNN방송 등에 따르면 FDA의 자문기구인 백신·생물의약품자문위원회(VRBPAC)는 이날 회의를 열고 J&J 백신의 안전성과 효능 등을 검토한 뒤 긴급사용 승인 권고를 결정했다. 현재까지 미국에서는 화이자·바이오엔테크와 모더나 백신 2종이 승인을 받아 사용되고 있다. FDA는 이르면 이날 밤중 J&J의 백신에 대해 긴급사용을 승인할 수도 있다고 CNN은 전망했다. 일반 접종을 위해서는 미 질병통제예방센터(CDC) 승인도 받아야 하는데, 이달 28일 CDC 자문기구의 표결이 예정돼 있다.
J&J 백신의 강점은 1회 접종으로 면역 효과가 생긴다는 것이다. 화이자·모더나 백신은 면역 효과를 위해 2회 접종이 필요하다. 일반 냉장고에 보관할 수 있어 보관도 용이하다. 미국과 남아프리카공화국 등에서 수행한 3상 임상시험 결과 평균 66%의 예방 효과를 보였다. 화이자(94%)나 모더나(95%)보다 낮은 수치지만, J&J 측은 이날 회의에서 "(화이자·모더나와 달리) 코로나19 변이 바이러스가 확산한 이후 임상시험을 수행했기 때문"이라고 설명했다. 실제 변이 바이러스가 확산된 남아공에서 64% 예방효과를 보여 다른 백신보다는 높은 성과를 보였다.
한편 유럽연합(EU)의 보건당국인 유럽의약품청(EMA)도 J&J 코로나19 백신 승인에 속도를 내고 있다. 블룸버그통신은 이날 익명의 EU 관리를 인용해 "EMA가 내달 11일 J&J 백신의 보건부 판매 승인 결정을 내릴 예정"이라고 전했다. EMA가 백신에 대한 판매 승인 권고를 하면 EU 행정부 격인 집행위원회가 최종 결정을 내리게 된다. 이후 EU 회원국들은 각각의 접종 방식와 일정을 정한다.
신고 사유를 선택해주세요.
작성하신 글을
삭제하시겠습니까?
로그인 한 후 이용 가능합니다.
로그인 하시겠습니까?
이미 공감 표현을 선택하신
기사입니다. 변경을 원하시면 취소
후 다시 선택해주세요.
구독을 취소하시겠습니까?
해당 컨텐츠를 구독/취소 하실수 없습니다.
댓글 0